
Jednostavni tehnički eksperimenti vrlo su korisni za djecu, to je provođenje vremena zajedno, usvajanje vještina i razumijevanje malih dizajnera, osnova, da hljeb, kao u čuvenom crtiću, ne raste na drveću.
Ovaj smo put odlučili napraviti najjednostavniji kemijski izvor struje i pokušati ga primijeniti za bilo što praktično. Kada govorimo o praktičnoj primjeni, vrijedno je podsjetiti da su samo prije nekoliko generacija radioamaterima, za opskrbu baterijskih prijemnika i pojačala, ponudili proizvodnju nekoliko vrsta galvanskih ćelija ili baterija za samostalnu proizvodnju. To su elementi Leklanshea i Popova [1], str. 9 ... 18, ili olovno-kalijeva ili plinska baterija [1], str. 22 ... 28. Nekoliko relativno strujnih elemenata bilo je spojeno na žarulju sa žarnom niti (žarulja sa žarnom niti), desetke manjih elemenata, na anodnu bateriju, čiji napon je mogao dostići 60-80 volti. Baterije su bile „mokre“ - s tekućim elektrolitom i bila im je potrebna njega i održavanje.
Dakle, galvanska ćelija, nekoliko riječi "kako?" i "zašto?" Električna struja nastaje kada metali djeluju. U tom slučaju dolazi do različite razlike potencijala (napona). Još 1793. godine Alessandro Volta, konstruirajući galvansku ćeliju (Volta stup), ustanovio je relativnu aktivnost tada poznatih metala: Zn, Pb, Sn, Fe, Cu, Ag, Au. Pokazalo se da je "snaga" galvanske ćelije veća, što su dalje metali u ovom nizu (niz napona).

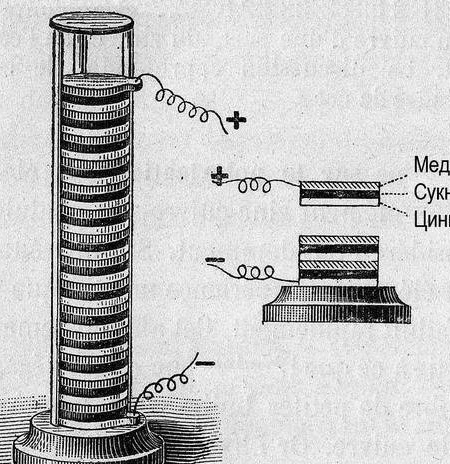
Kasnije, za organiziranje podataka, iskorišten je potencijal "vodikove elektrode" za nulte reference. Nakon mjerenja potencijala metala uparenih s njim, eksperimentalni metali su raspoređeni u nizu. Rezultirajuća tablica nazvana je "Elektrokemijska serija metalnih naprezanja", a u kabinetu za kemiju mora visiti pored periodičnog sustava i portreta Dmitrija Ivanoviča.
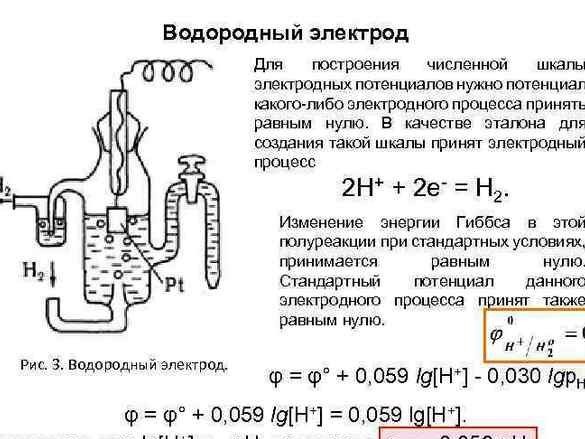

Brojni naponi metala korisna su kontracepcija, u našem slučaju ćemo i mi, poput Alessandra Volta, znati - što se metali dalje odvajaju jedan od drugog, to će se postići veća napetost.
U našim smo eksperimentima, poput klasika, koristili bakar i cink.Kad su ploče uronjene u elektrolit, između njega i cinkove ploče, dolazi do kemijske reakcije, posljedica koje se na ploči nakupljaju negativni naboji i negativno se nabija. Kao rezultat reakcije koja se odvija u galvanskoj ćeliji, cinkova elektroda se postupno rastvara.
Na bakrenoj elektrodi tijekom rada galvanske ćelije formiraju se sitni vodikovi mjehurići koji izoliraju površinu bakra od elektrolita. Fenomen se zove, u galvanskoj ćeliji je štetan, oni se s njim bore. Za uklanjanje oslobođenog vodika, tvari koje se nazivaju vodik uvode se u elektrolit. U njihovoj ulozi često su spojevi mangana, bakrenog sulfata. U jednostavnim eksperimentima može se koristiti ljekarni kalijev permanganat.
Što smo koristili za eksperiment.
Uređaji i materijali.
Za sastavljanje galvanskih ćelija, kao bakrene elektrode, možete koristiti žicu, žicu, foliju. Cink se može ekstrahirati iz suhih elemenata, mogu se koristiti pocinčani proizvodi. Umjesto cinka, možete pokušati koristiti elektrodu od aluminija ili željeza. Natrijev klorid za elektrolit, malo mekane žice za ugradnju. Svakako vam trebaju voltmetar ili multimetar, rezači žica, škare. Kao posude mogu se koristiti nemetalni spremnici odgovarajuće veličine. Staklena, prikladnija od lakih plastičnih čaša - teže su, stabilnije i teže ih je razbiti. Vrlo je dobro ako postoji opterećenje niskog napona niskog napona - jednostavan radio, kvarcni sat itd.
"Visokonaponska" baterija od žica i vijaka.
Fascinirani jednostavnošću detalja i relativno visokim primljenim naponom pokušali smo sastaviti takvu bateriju. Ovdje se koristi "klasični" par metala - bakar-cink. Ideja je koristiti pocinčane pričvršćivače kao cinkovu elektrodu. Graciozno. Jasno je da takav element nije dizajniran za dugotrajni rad - tanki sloj cinka brzo će se rastopiti, međutim, to nije važno za kratkotrajni eksperiment. Ali pocinčani vijci ili zupčanici su svugdje puni.
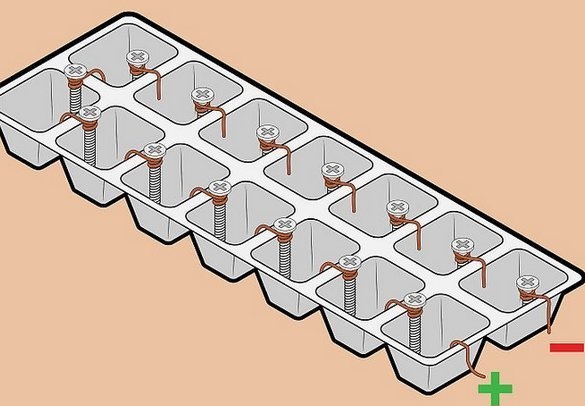
Žica se koristi i kao bakrena elektroda - također široko dostupan materijal, uz to - najpovoljnija instalacija elemenata u bateriji - svi su elementi povezani serijski - plus jedan do minus sljedećeg. U tom se slučaju napon zbraja, struja ostaje ista.
Počnimo.
Nakon odabira potrebnog broja pocinčanih pričvršćivača željene duljine, pronašli smo prikladnu bakrenu žicu. Ovo je žica za namatanje u izolaciji lakova. Promjer žice je oko 0,5 mm.

Stup nekoliko puta čisti izolaciju laka, naprežući žicu kroz dvostruko presavijenu brusnu krpu srednje veličine.


Zatim, priprema par elektroda - ispod glave samoreznog vijka, čvrsto omota dva ili tri okretaja žice i odreže višak.

Sklop baterije - korito je korišteno kao spremnik za zamrzavanje leda. Možete koristiti ćelije iz kutijastih slatkiša, međutim, one su suptilnije. Nakon ugradnje elektroda na zidove između stanica, spremnike napunimo elektrolitom. Koristili smo otopinu kuhinjske soli - žlicu s toboganom od 0,5 litara tople vode. Za punjenje je vrlo prikladno koristiti medicinsku štrcaljku.


Pronašli smo još nekoliko vijaka za elektrode i dodali elemente na bateriju, to je ono što imamo. Napon pri visokom impedancijskom opterećenju (ulazni otpor digitalnog voltmetra) je značajan, ali pri svakom opterećenju, koliko god primjetno, znatno pada.
Pokušaj učiniti slična galvanska ćelija (baterija) s većim elektrodama.
Kao spremnik koristili smo staklenku od pola litre (dvije), u nju će se uklopiti tanjuri znatnog područja. Kao elektrode uzeli smo tanku bakrenu foliju i cink - ostatke čaše iz tvorničkih "suhih" elemenata, rastavljenih tijekom proizvodnje grafita za vatrostalni premaz.

Ostatke osušenih kristalnih soli očistili smo žičanom četkom i rezali dvije ploče s približno škarama s približno istim područjem. Iz bakrene folije izrežite dvije odgovarajuće trake. Također sa škarama. Dobili smo dva para elektroda koje su opremile naše elemente, bez dodatnog divljenja, savijajući njihove rubove na vratu limenke.


U većoj posudi pripremili su elektrolit - natrijev klorid, otopljen u toploj vodi, koncentracija je ista i pripremljeni elementi se sipaju.


Dva elementa u nizu povezali smo pomoću komada žice za montažu i dva kopče za krokodile. Dakle, u redu, napon baterije je blizu standardnog "prsta", pokušajte koristiti. Jedan element s naponom od 1,5 V koristi se u elektromehaničkom satu, osim toga, trenutna potrošnja sata je vrlo mala i naša baterija će ga moći nadjačati.

Izvadili smo standardnu bateriju s sata i spojili na terminale komad žice za montažu. Promatrajući polaritet (bakrena ploča - "+", cink - "-"), povezali smo sat s improviziranom baterijom, voila! Sat djeluje, napon "tone" na 1,3 V. Sat je savršeno funkcionirao nekoliko sati, sve dok se svi nismo pohvalili (ma koji je čarobnjak!), A onda smo se umorili.

Na stazu.
Unutarnja konstitucija bilo kojeg djeteta je takva da se pažnja na jedan predmet može usredotočiti ne više od 15 ... 20 minuta, a sve časove s djecom treba isplanirati tako da se u to vrijeme uklapaju ili prelaze između različitih razreda, jer ćete se u protivnom obojica mučiti.
Kao opterećenje je bolje primijeniti bilo da se kreće ili svijetli - brojevi na voltmetru impresioniraju um, ali ne i srce. Osim satova i kalkulatora, zasigurno će izazvati divljenje, rad iz kućne baterije malog radijskog prijemnika (kao opcija - kućni rad!).
Za dugotrajnu upotrebu, elektrolit stanica treba zaštititi od prašine i isparavanja, paziti i na depolarizator - dobro, barem začepiti staklenku komadićem plastičnog filma s elastičnom trakom i dodati kalijev permanganat u elektrolit. Štoviše, bolje je odmah prikupiti spomenuti Popov element.
Osim pocinčanih samoreznih vijaka, moguće je koristiti pocinčani čelični lim, za velike elemente je prikladnije - tijekom eksperimenta možete dobiti značajnu struju i snagu bez obzira (pomičući prste u zraku).
Popis rabljene literature.
1. P. Strelkov. Znati i moći. Pionirski inženjer elektrotehnike. Detgiz. 1960. godina
2. V. S. Polosin, V. G. Prokopenko. Radionica o metodologiji poučavanja kemije. Moskva, "Prosvjetiteljstvo", 1989., str. 202.203.

